Durante las primeras semanas de vida, cada decisión médica en torno a un bebé prematuro puede tener consecuencias duraderas. Uno de los desafíos más importantes en la salud de estos pequeños es el desarrollo pulmonar: nacen antes de que sus pulmones hayan completado su maduración y eso aumenta el riesgo de sufrir dificultades respiratorias a corto y largo plazo. Ahora, un nuevo estudio ha abierto una puerta prometedora al demostrar que un sencillo ajuste en los cuidados respiratorios puede marcar un gran impacto diferencial.
La investigación, publicada en la revista científica American Journal of Respiratory and Critical Care Medicine, evaluó los efectos de prolongar una técnica respiratoria no invasiva en bebés prematuros durante sus primeras semanas de vida. Los resultados, según los investigadores, han sido muy claros: los pulmones de estos bebés neonatos crecieron mejor y funcionaron de forma más eficaz a los seis meses de edad corregida, en comparación con otros bebés que recibieron la misma técnica durante un periodo más breve.
Aunque la intervención médica se llevó a cabo en un entorno hospitalario y especializado, las implicaciones que tiene para las familias son enormes. En un momento en el que los padres viven con angustia la fragilidad de sus hijos prematuros, contar con evidencias científicas que respalden prácticas seguras y eficaces supone un paso vital para ofrecerles un mejor pronóstico y tranquilidad a largo plazo.
Cómo puede cambiar la evolución de los bebés prematuros
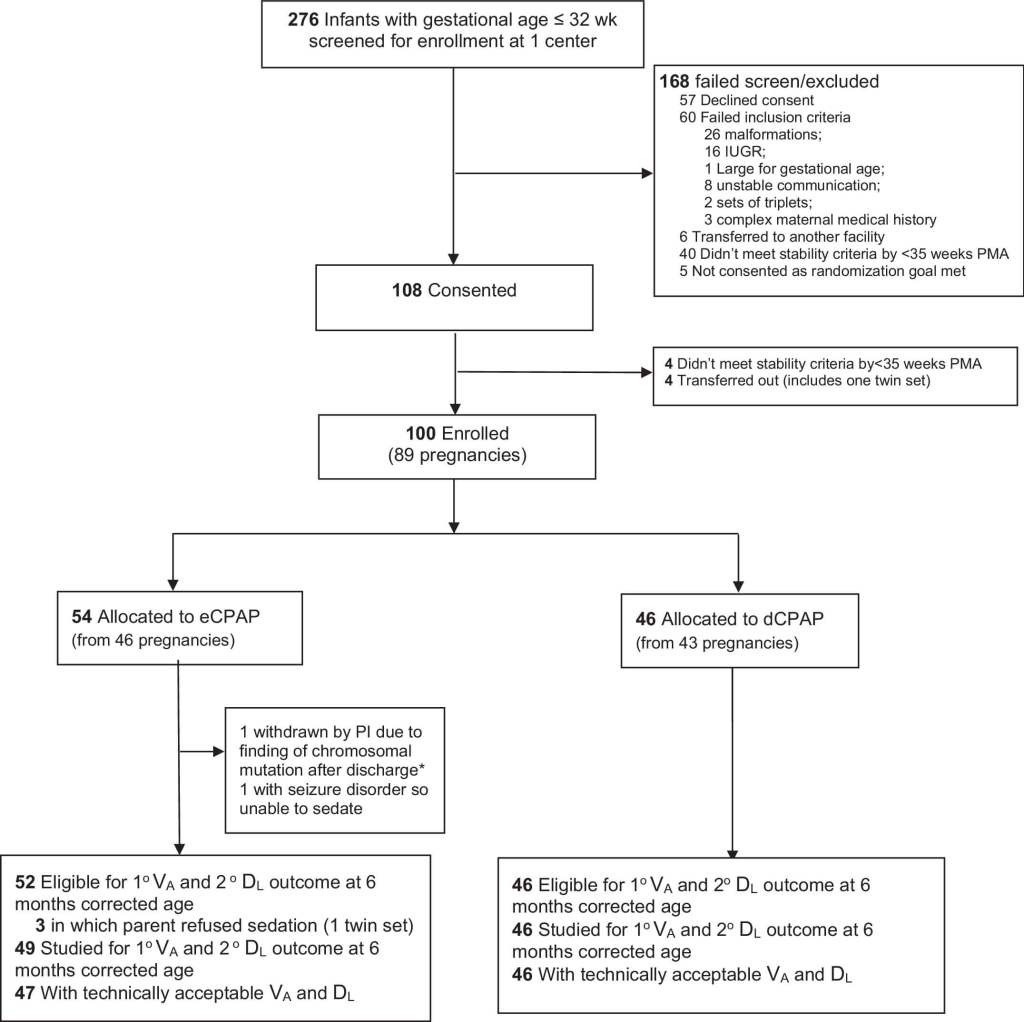
El ensayo clínico dirigido por la Dra. Cindy McEvoy, experta en neonatología y profesora en la Oregon Health & Science University, se llevó a cabo con 204 bebés nacidos antes de la semana 28 de gestación en hospitales de Estados Unidos. Todos los bebés participantes necesitaron asistencia respiratoria tras el nacimiento, una situación frecuente en este grupo. Pero el elemento diferencial del estudio fue el tiempo durante el cual se aplicó un soporte respiratorio continuo no invasivo, un tipo de ayuda que mantiene los pulmones ligeramente abiertos para facilitar el intercambio de oxígeno.
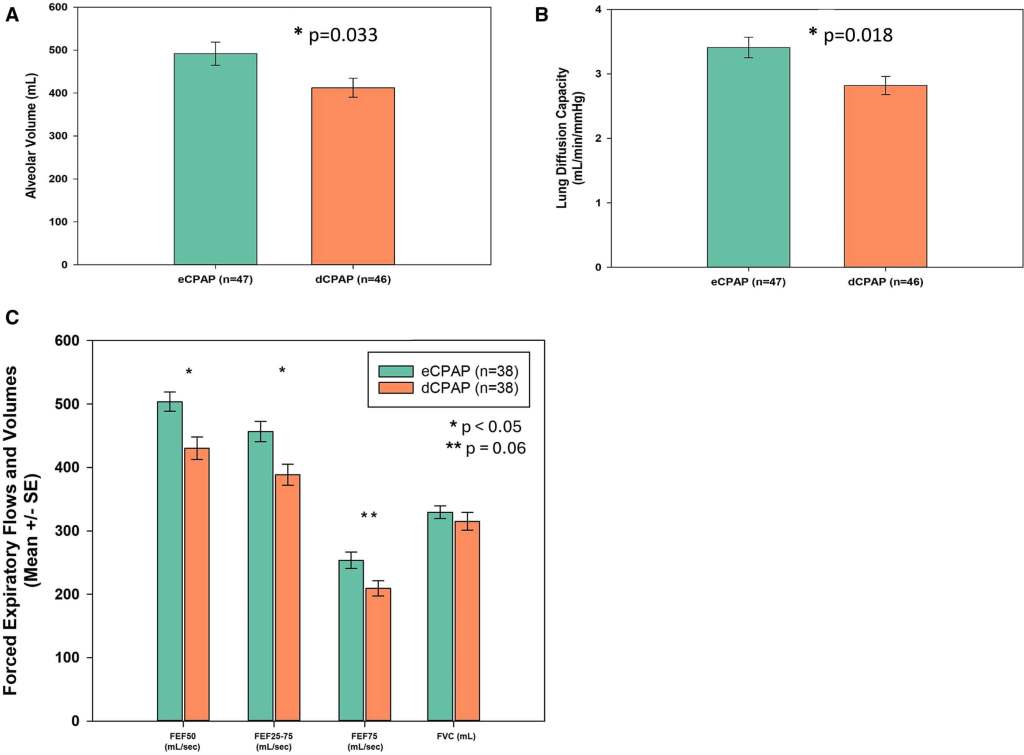
Los investigadores dividieron a los bebés en dos grupos: uno recibió esta asistencia durante aproximadamente un mes, mientras que al otro se le mantuvo este soporte durante más de dos meses. Lo llamativo es que, sin necesidad de recurrir a técnicas invasivas o tratamientos farmacológicos adicionales, los bebés del segundo grupo mostraron pulmones más grandes y una función respiratoria más eficiente a los seis meses, evaluados mediante pruebas de imagen y funcionales.
En cifras concretas, los bebés que recibieron la intervención prolongada tuvieron un 22% más de volumen pulmonar ajustado por peso corporal, y un 28% menos de episodios de sibilancias o necesidad de medicación respiratoria. Además, presentaron una reducción significativa en los ingresos hospitalarios por infecciones respiratorias.
“Hemos demostrado que pequeños cambios en la duración del soporte respiratorio pueden producir un efecto duradero en la salud pulmonar de los bebés más vulnerables”, afirma la autora principal del estudio, la doctora McEvoy.
Aplicaciones para la crianza y la salud infantil
Aunque la técnica utilizada en el estudio es propia de unidades neonatales especializadas, su impacto se traduce en mejoras reales en el desarrollo respiratorio de los bebés prematuros. Esto se traduce, a su vez, en una reducción de la ansiedad que sufren muchas familias en los primeros meses tras el alta hospitalaria.
En contextos donde las enfermedades respiratorias son la principal causa de hospitalización infantil —como bronquiolitis o infecciones de vías respiratorias bajas—, mejorar desde el principio la estructura y la función de los pulmones puede suponer un antes y un después. Menos ingresos, menos medicación, y una mejor calidad de vida para los bebés y sus familias.
Este hallazgo también puede abrir un nuevo campo de conversación entre padres y profesionales de neonatología. Aunque cada caso es único, el estudio plantea que algunas prácticas hospitalarias podrían adaptarse para priorizar intervenciones de menor impacto físico pero con grandes beneficios a medio y largo plazo.
Además, investigaciones como esta sirven para visibilizar el papel crucial de la ciencia en etapas tempranas del desarrollo. Tal y como ocurrió con otros descubrimientos en salud perinatal —como el contacto piel con piel o el uso de leche materna en unidades neonatales—, esta intervención aparentemente técnica puede transformarse en una recomendación clínica clave.
Referencias
- McEvoy C., Collaco J.M., Aschner J.L., et al. Extended Continuous Positive Airway Pressure in Preterm Infants Increases Lung Growth at 6 Months: A Randomized Controlled Trial. American Journal of Respiratory and Critical Care Medicine, 2025. DOI: 10.1164/rccm.202411-2169OC




