En un laboratorio australiano, un grupo de científicos ha logrado lo que durante años parecía inalcanzable: observar en tiempo real cómo ciertos genes afectan directamente al desarrollo de la placenta humana. Lo han hecho creando “mini placentas” en placas de cultivo, una técnica de vanguardia que, más allá del logro técnico, ha puesto el foco sobre un gen que hasta hace poco solo era famoso por su papel en la pandemia de COVID-19: ACE2.
Lo que estos investigadores han encontrado podría cambiar la forma en que entendemos el embarazo y, sobre todo, las causas detrás de algunas de sus complicaciones más peligrosas. Preeclampsia, retraso en el crecimiento fetal o nacimientos de bebés más pequeños de lo esperado para su edad gestacional son algunos de los problemas que, según este nuevo estudio, podrían estar influenciados directamente por variaciones en ese gen.
Pero ¿cómo es posible que un gen vinculado a un virus respiratorio pueda también decidir el destino de un embarazo? La respuesta está en los complejos equilibrios moleculares que regulan la vida antes incluso del nacimiento.
El sistema oculto que mantiene con vida al feto
El gen ACE2 forma parte del sistema renina-angiotensina, una red hormonal fundamental para controlar la presión arterial y el equilibrio de líquidos en el cuerpo. Este sistema tiene dos brazos opuestos: uno que promueve el crecimiento celular y la inflamación (mediado por la enzima ACE) y otro que actúa como freno, con efectos antiinflamatorios y de regulación del crecimiento (dirigido por la ACE2). En condiciones normales, estos dos brazos se equilibran.
Pero en la placenta, donde cada célula y cada molécula están milimétricamente programadas para sostener la vida en desarrollo, un pequeño desequilibrio puede tener consecuencias catastróficas.
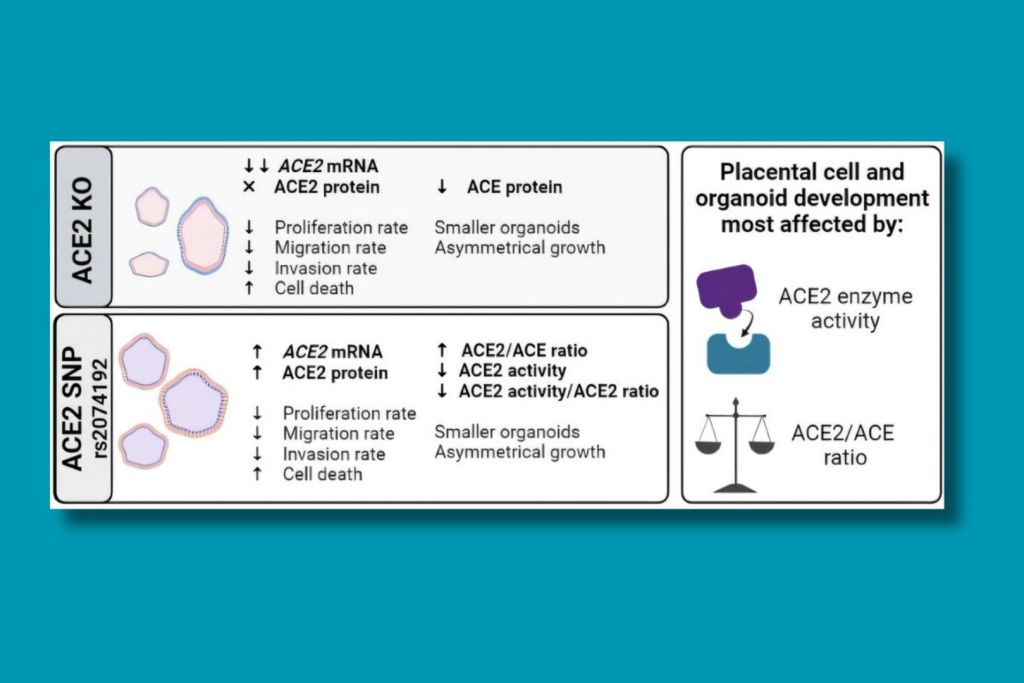
El hallazgo más llamativo del estudio es que tanto la ausencia del gen ACE2 como ciertas variantes genéticas del mismo provocan alteraciones visibles en el desarrollo placentario. Los organoides con el gen eliminado crecieron menos, de forma irregular, y mostraron más muerte celular. Por otro lado, aquellos que contenían la variante genética conocida como rs2074192 —presente en más de un tercio de la población mundial— mostraron una actividad reducida de la enzima ACE2, a pesar de que sus niveles de proteína eran mayores. Un funcionamiento anómalo disfrazado de aparente normalidad.
Una puerta de entrada y una puerta al futuro
El gen ACE2 se hizo conocido por ser la puerta de entrada del coronavirus SARS-CoV-2 en las células humanas. Pero lo que muchos no saben es que, mucho antes de la pandemia, ya había estudios que lo vinculaban a la salud materna. Las mujeres embarazadas producen más ACE2 de lo habitual, y su desequilibrio ha sido relacionado con preeclampsia, un trastorno grave que eleva la presión arterial y puede dañar órganos vitales de la madre.
Este nuevo estudio no solo refuerza esa sospecha, sino que da un paso más: demuestra con precisión qué ocurre cuando el sistema se altera desde el mismo momento de la concepción.
Para ello, los investigadores emplearon herramientas de edición genética para modificar células madre obtenidas de placentas humanas en las primeras semanas de gestación. A partir de esas células crearon organoides, pequeños modelos tridimensionales que imitan el comportamiento de una placenta real. No es ciencia ficción, sino ciencia en su estado más avanzado.
Una genética que no perdona
Uno de los aspectos más reveladores del estudio es la implicación de una simple variante genética —un cambio de una sola letra en el ADN— que puede aumentar 23 veces el riesgo de que un bebé nazca con un peso inferior al esperado. Y lo más inquietante: esa variante no necesita estar en la madre para causar problemas. Basta con que el feto la herede, ya que la placenta comparte el mismo material genético que el embrión.
Este hallazgo introduce una nueva dimensión en la medicina maternofetal. Hasta ahora, muchos estudios se centraban en el entorno uterino y en los hábitos de la madre. Pero cada vez resulta más evidente que los genes del feto también juegan un papel decisivo en la salud del embarazo.
Aunque el estudio está lejos de traducirse en tratamientos clínicos inmediatos, abre una puerta esperanzadora para futuras terapias personalizadas. Conocer la arquitectura genética de la placenta y su comportamiento molecular podría permitir, en un futuro no tan lejano, intervenir de forma precisa en embarazos de riesgo, quizás incluso antes de que aparezcan los primeros síntomas.
Al mismo tiempo, plantea preguntas profundas sobre la necesidad de realizar pruebas genéticas prenatales más detalladas. Si una simple variante puede modificar el desarrollo de la placenta, ¿deberíamos empezar a rastrearlas sistemáticamente?
Una nueva frontera para la medicina del embarazo
En un mundo donde las tasas de preeclampsia y nacimientos con bajo peso siguen preocupando a los sistemas de salud, este avance marca el inicio de una nueva era. Ya no se trata solo de observar ecografías o controlar la presión arterial. Ahora es posible mirar dentro del funcionamiento íntimo de la placenta y entender, desde sus primeros días de vida, qué puede salir mal y por qué.
Las mini placentas creadas en laboratorio han demostrado ser algo más que un logro técnico: son una ventana al futuro de la medicina del embarazo. Y lo que muestran es tan fascinante como inquietante.
Referencias
- Arthurs, A.L., Dietrich, B., Knöfler, M. et al. Genetically edited human placental organoids cast new light on the role of ACE2. Cell Death Dis 16, 78 (2025). DOI: 10.1038/s41419-025-07400-x




